علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
التجربة ( 1)
المؤلف:
م.مسعود فرج ابو ستة
المصدر:
تجارب في الكيمياء التحليلية (التحليل الكمي الحجمي والوزني )
الجزء والصفحة:
ص70
25-1-2016
2779
تطبیقات عملیة على معایرات التعادل (التجارب العملیة)
التجربة ( 1)
معایرة محلول من هیدروكسید الصودیوم مجهول التركیز مع محلول قیاسي من الهیدروكلوریك N 0.15 عیاري.
الهدف من التجربة:
حساب عیاریة وكمیة هیدروكسید الصودیوم والتركیز بالوحدات المختلفة في محلول العینة المجهولة بأستخدام دلیل المیثیل البرتقالي والفینول نفثالین .
HCl+ NaOH → NaCl+ H2O معادلة التفاعل
المواد والأدوات المطلوبة:
- محلول حمض الهیدروكلوریك(HCl ) قیاسي تركیزه N 0.15عیاري . والحصول على محلول قیاسي من حمض الهیدر وكلوریك بدقة صعب لأنه مادة قیاسیة ثانویة ولكي یستخدم كمحلول قیاسي في المعایرة یتم ضبط عیاریته،حیث یتم معایرته بواسطة محلول قیاسي أولي مثل (Na2CO3) كربونات الصودیوم بأستخدام دلیل المیثیل البرتقالي
- محلول عینة مجهولة من هیدروكسید الصودیوم.
- دلیل فینول نفثالین.
- سحاحة حامل السحاحة ماصة قیاسیة حجم 25 و 50 مل . دورق مخروطي سعة 250 مل .كأس سعة 400 مل. ساق زجاجیة.
خطوات التجربة:
- نظف أدوات التجربةبالماء العادي ثم الماء المقطر.
- اغسل السحاحة بعد غسلها بالماء المقطر بكمیة قلیلة من محلول هیدروكسید الصودیوم المستعمل في المعایرة،للتخلص من قطرات الماء الملتصقة بجدارها من الداخل عند غسلها بالماء المقطر.
- إملاء السحاحة بمحلول هیدروكسید الصودیوم واظبط الحجم علي صفر التدریج ،ویجب التأكد من شیئین أحدهما امتلاء الجزء السفلي من السحاحة (ما تحت الصنبور) ، وثانیهما عدم وجود فقاعات هوائیة داخل السحاحة .
- انقل بالماصة القیاسیة حجم من محلول حمض الهیدروكلوریك القیاسي 0.15 N مقداره 25 مل إلى الدورق المخروطي أضف إلى الدورق قطرتین أو ثلاث من دلیل الفینول نفثالین ولاحظ ماذا یحدث للمحلول .
- إبداء عملیة المعایرة بتنقیط محلول NaOH من السحاحة علي الدورق المخروطي قطرة قطرة مع الرج المستمر،واستمر في المعایرة حتى یتغیر لون المحلول إلى اللون الوردي ، وسجل الحجم المستهلك من السحاحة وليكن . VA
- كرر الخطوات السابقة بعد أن تغسل دورق المعایرة جیداً بالماء العادي ثم المقطر وسجل الحجم المستهلك من السحاحة ولیكن VB , اعد خطوات التجربة مستخدماً دلیل المیثیل البرتقالي ثم قارن بین العیاریة في حالة الدلیلین.
الحسابات:
یتم حساب متوسط الحجم لهیدروكسید الصودیوم (V1)
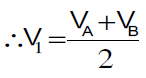

نفرض أن الحجم 3.9 مل V1 =


 الاكثر قراءة في التحليل النوعي والكمي
الاكثر قراءة في التحليل النوعي والكمي
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)